撰文 | 刘一都(2024级博士研究生)
审核 | 李国民
背景介绍
肿瘤免疫治疗为癌症治疗带来了革命性的变化,为各种类型的癌症患者提供了新的希望。CD8+ T细胞的效应功能或者说它的细胞毒性是癌症免疫治疗的核心。然而,许多患者对免疫治疗反应不佳,一个主要原因是肿瘤微环境通过限制T细胞的浸润、损害T细胞的维持和抑制效应功能来麻痹抗肿瘤免疫反应[1]。
最近的研究表明,肿瘤微环境中的离子失衡可能是限制T细胞效应功能的重要因素[2]。例如,有研究发现K+在坏死的肿瘤微环境中富集,这提示K+可作为肿瘤诱导的离子检查点影响T细胞效应功能[3]。升高的Na+浓度被证明能强烈促进Th17细胞的分化和Th2细胞对mTORC2信号通路的反应[4-5]。最近,Na+也被证明可以通过扰动线粒体呼吸破坏调节性T细胞的免疫抑制功能[6]。然而,Na+对CD8+ T细胞的直接作用,以及对其抗肿瘤细胞毒性的影响尚不清楚。近期德国Leibniz 研究所的Christina E. Zielinski教授团队研究发现,肿瘤微环境中的氯化钠能增强T细胞的代谢适应性和细胞毒性。相关成果于2024年8月28日发表在国际知名学术期刊《自然—免疫学》。本期的Journal Club将对这项研究给大家做一个详细的介绍。
研究结果
1. 肿瘤微环境中钠含量增加
文章首先发现了在乳腺癌患者中,癌组织的钠钾离子浓度显著高于癌旁组织。他们通过分离健康供体外周血中的CD8+CD45RA-的T细胞进行高氯化钠与低氯化钠处理,将高盐处理上调表达的基因集命名为“氯化钠标签”。研究发现“氯化钠标签”在二十多种实体瘤癌症以及乳腺癌肿瘤浸润CD8+淋巴细胞中有富集,表明高氯化钠状态确实会在肿瘤浸润淋巴细胞中留下转录印记。
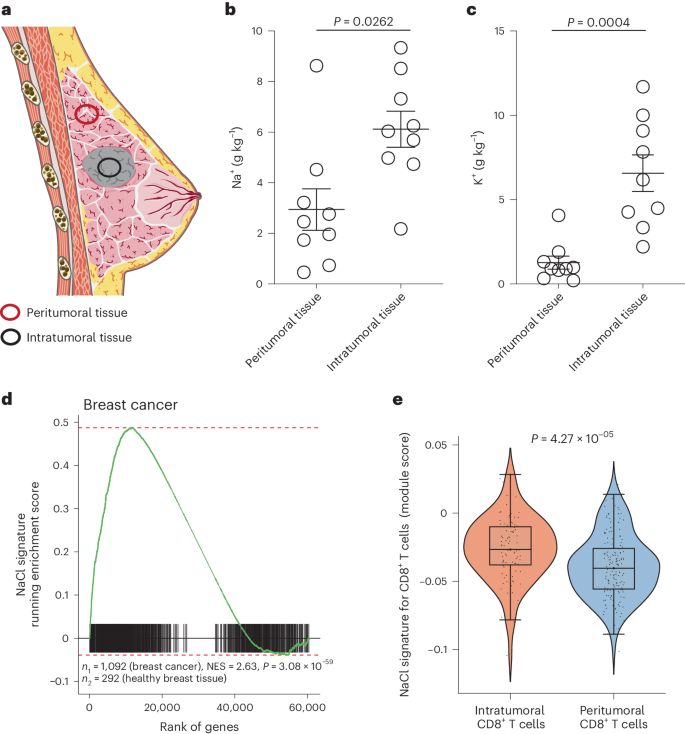
图1 NaCl在实体瘤中高度富集并留下转录印记
2. 氯化钠增强CD8+ T细胞的活化及TCR信号转导
随后他们探究了高盐对于T细胞活化及效应功能的影响。全转录组测序结果显示高盐改变了CD8+CD45RA- T细胞的整体转录状态,多个与T细胞活化、代谢以及效应功能相关的基因表达水平显著上调。单细胞转录组数据也显示高盐处理的T细胞在“活化、增殖、分化与效应功能”等信号通路富集聚类,并且T细胞活化与TCR信号通路及其下游相关基因的表达明显增强,高盐同时增强了TCR刺激诱导的钙离子内流。
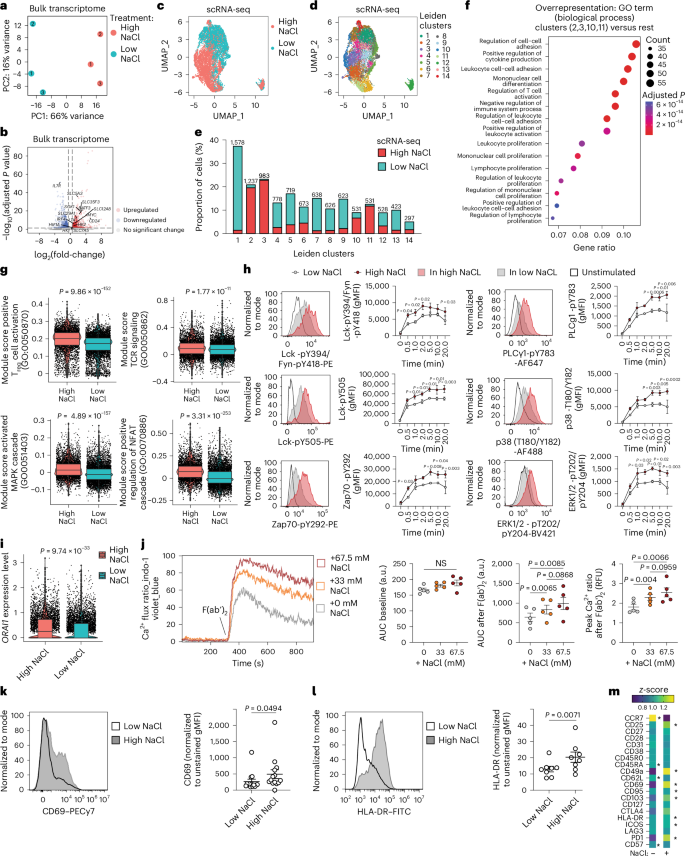
图2 NaCl可增强人CD8+记忆T细胞的活化状态
3. 氯化钠能增强细胞毒性T细胞杀伤功能
对转录组数据进一步分析发现,在高NaCl条件下,CD8+ T细胞表现出明显的效应细胞特征,细胞干性特征降低。细胞分化轨迹分析显示CD8+ T细胞是从低盐到高盐逐渐转变的。另外高盐条件下CD8+ T细胞分泌的细胞因子以及毒性分子水平升高。
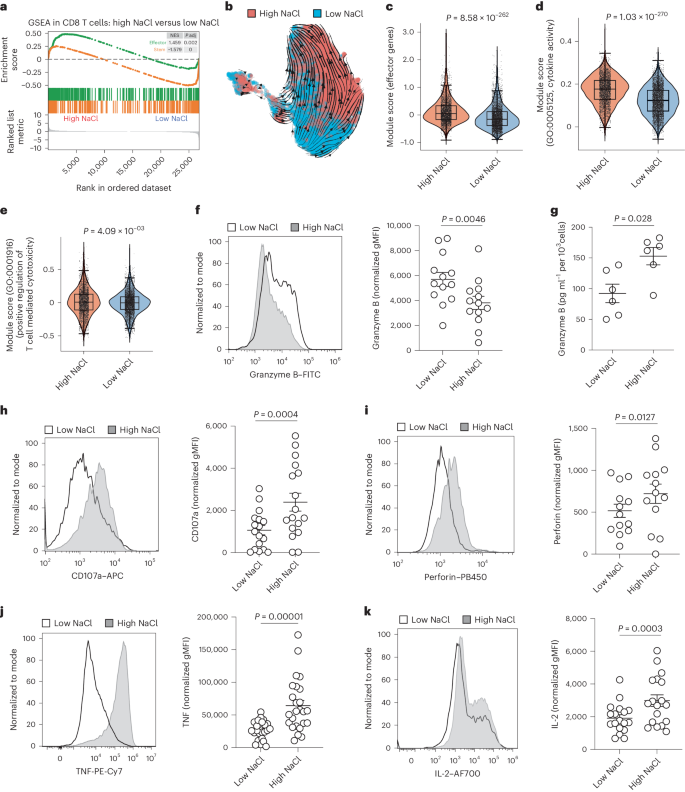
图3 NaCl增强CD8+ T细胞的效应功能和细胞毒性
4. 氯化钠能增强CD8+ T细胞的代谢适应能力
氯化钠为何能增强CD8+ T细胞杀伤功能?代谢重编程被认为是一个可能的机制,他们对高氯化钠条件ATP生成、几种主要营养物质转运量以及转运蛋白表达量、氧化磷酸化等多方面进行了分析,发现在高氯化钠条件下,这些过程都显著增强的增强起促进作用,并且mTOR通路也被活化。
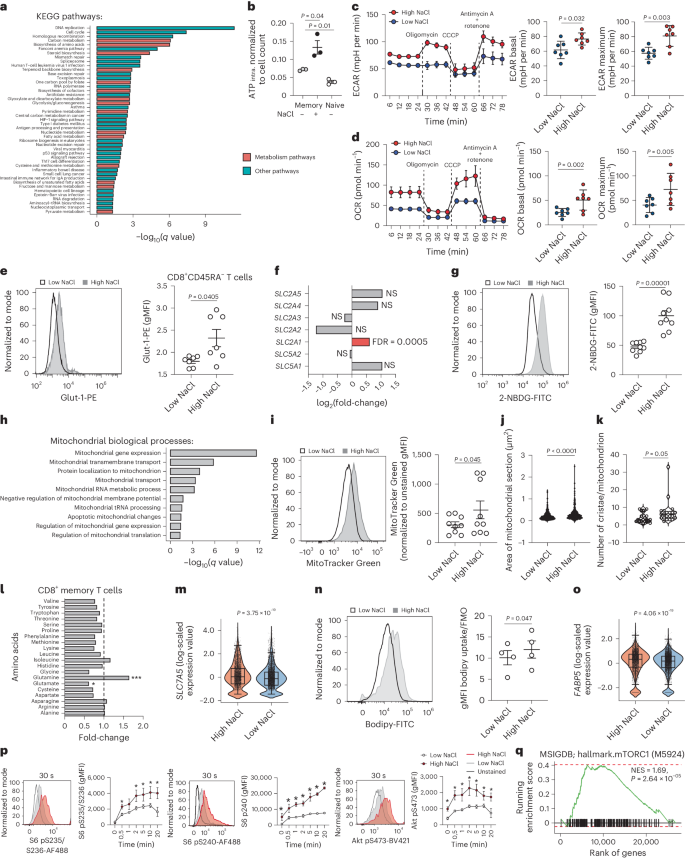
图4 NaCl可增强CD8+ T细胞的代谢适应性
5. 氯化钠通过Na+/K+-ATP酶使膜电位超极化
紧接着他们发现是高Na+引起的Na+/K+-ATP酶的激活导致的细胞膜相对超极化,增强了TCR激活诱导的钙离子内流。使用Na+/K+-ATP酶的抑制剂Ouabain则会减弱钙离子内流,降低高氯化钠存在时mTOR信号的激活与毒性因子释放。他们由此得出以下机制:高NaCl条件下,Na⁺内流增加,导致细胞内Na⁺浓度升高,进而增强Na⁺/K⁺- ATP酶活性,这有助于维持细胞膜的超极化状态,从而增强TCR激活过程中钙离子内流,钙离子一方面诱导NFAT活化,另一方面激活mTOR信号通路,增强细胞对葡萄糖、谷氨酰胺和脂肪酸的摄取,诱导代谢重编程,促进ATP的快速生成,细胞因子的产生和细胞毒性分子颗粒酶B的分泌,增强T细胞的效应功能,提高杀伤肿瘤细胞的能力。
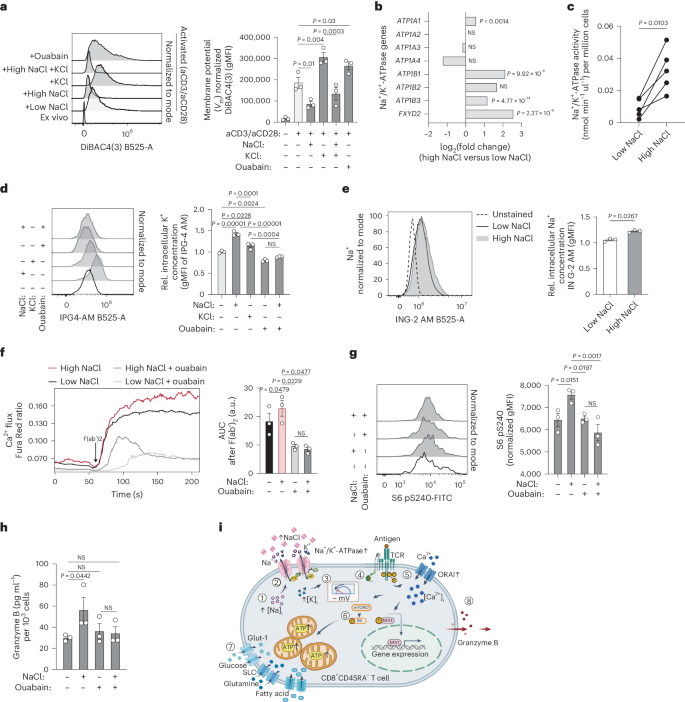
图5 NaCl通过Na+/K+-ATP酶增强膜超极化
6. 高氯化钠可在人类和小鼠体内促进T细胞对肿瘤细胞的杀伤
最后,他们通过体外CAR-T与体内小鼠实验测试并证实了高NaCl处理的T细胞的具有高效杀伤能力。他们通过对小鼠和人类肿瘤微环境中T细胞的分析,发现NaCl的存在与T细胞的细胞毒性增强有关。
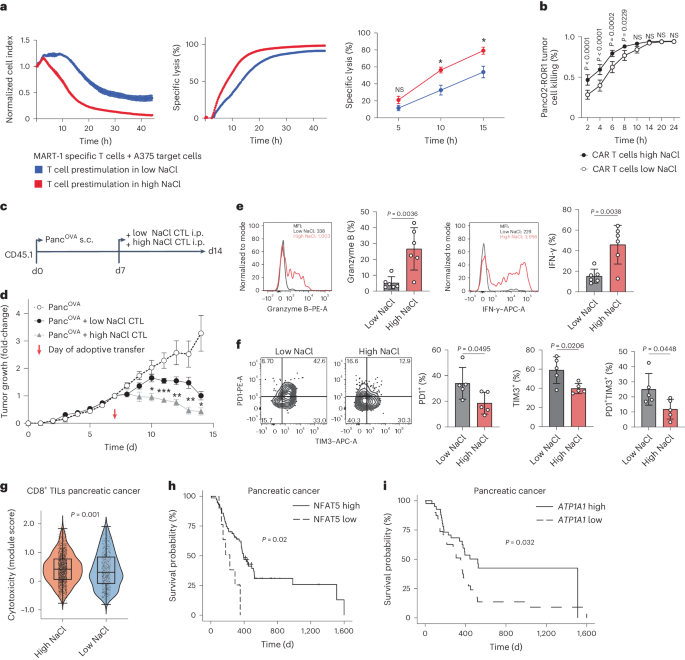
图6 NaCl可使CD8+ T细胞在体内外杀灭肿瘤细胞
总结
综上,该文章作者发现了肿瘤微环境中的高NaCl浓度对细胞代谢产生显著影响,并通过Na+/K+-ATP酶依赖的分子机制增强CD8+ T细胞的效应功能,提升了T细胞抗肿瘤毒性。并且NaCl有助于增强T细胞过继疗法的细胞毒性,为肿瘤免疫治疗以及依赖于T细胞毒性的疾病提供了崭新的治疗策略。
不过文章仍有一些局限之处,包括以下两个方面:
1. 肿瘤微环境中持续的NaCl沉积可能潜在地促进T细胞衰竭。
2. 高NaCl可能对心血管疾病等产生不良影响,需要更多的临床试验来评估NaCl对抗肿瘤免疫的短期和长期影响。
总体来说,该文章加深了我们对 CD8+ T细胞调控的理解,揭示了调节T细胞活化的新机制。
原文链接
DOI: 10.1038/s41590-024-01918-6
参考文献
[1] DePeaux K, Delgoffe GM. Metabolic barriers to cancer immunotherapy. Nat Rev Immunol. 2021;21(12):785-797.
[2] Eil R, Vodnala SK, Clever D, et al. Ionic immune suppression within the tumour microenvironment limits T cell effector function. Nature. 2016;537(7621):539-543.
[3] Vodnala SK, Eil R, Kishton RJ, et al. T cell stemness and dysfunction in tumors are triggered by a common mechanism. Science. 2019;363(6434):eaau0135.
[4] Wu C, Yosef N, Thalhamer T, et al. Induction of pathogenic TH17 cells by inducible salt-sensing kinase SGK1. Nature. 2013;496(7446):513-517.
[5] Matthias J, Maul J, Noster R, et al. Sodium chloride is an ionic checkpoint for human TH2 cells and shapes the atopic skin microenvironment. Sci Transl Med. 2019;11(480):eaau0683.
[6] Côrte-Real BF, Hamad I, Arroyo Hornero R, et al. Sodium perturbs mitochondrial respiration and induces dysfunctional Tregs. Cell Metab. 2023;35(2):299-315.e8.