
王宇涛实验室聚焦核受体家族成员在抗病毒感染与肿瘤治疗中的功能及转化潜力,致力于解析其转录与非转录依赖调控机制,阐明其在天然免疫活化、溶瘤病毒复制与免疫逃逸,以及肿瘤免疫微环境建立与重塑中的作用。实验室综合运用CRISPR 筛选、多组学分析、合成生物学和小分子化合物筛选等策略,系统发掘关键可成药靶点,并开发机制驱动的联合干预方案,以提升抗病毒和抗肿瘤治疗的整体疗效。
主要研究课题
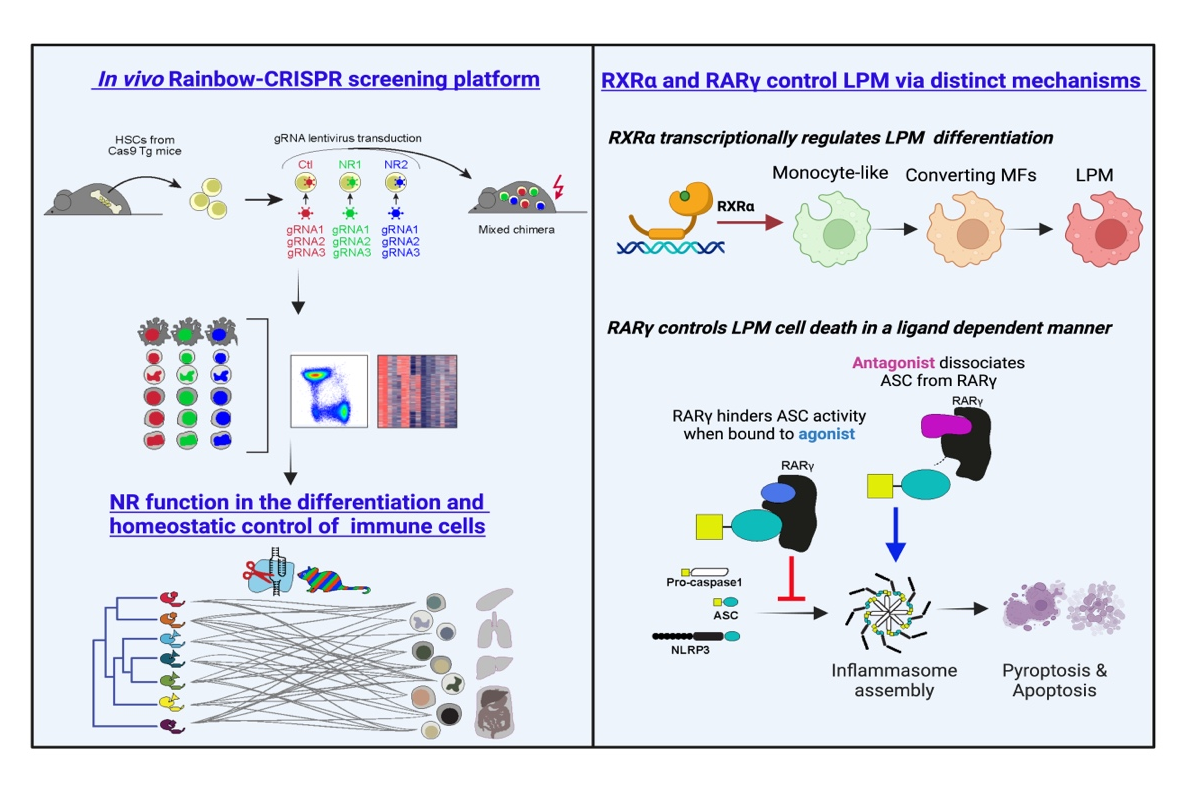



Wang Y, Zhang Y, Kim K, Han J, Okin D, Jiang Z, Yang L, Subramaniam A, Means TK, Nestlé FO, Fitzgerald KA, Randolph GJ, Lesser CF, Kagan JC, Mathis D, Benoist C. A pan-family screen of nuclear receptors in immunocytes reveals ligand-dependent inflammasome control. Immunity, 2024, 57: 2737-2754. DOI: 10.1016/j.immuni.2024.10.010.
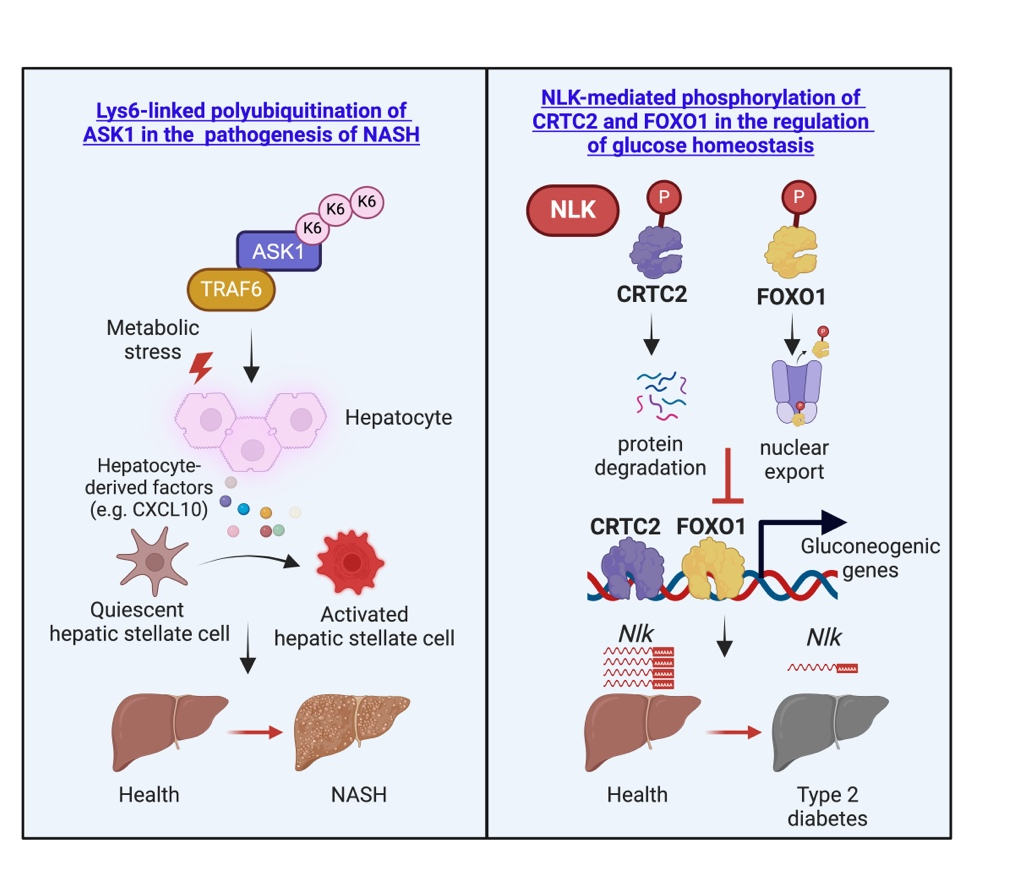
Ji YX*, Wang Y*, Li PL*, Cai L*, Wang XM, Bai L, Liu Z, Tian H, Tian S, Zhang P, Zhang XJ, Cheng X, Yuan Y#, She Z#, Li H#. A kinome screen reveals that Nemo-like kinase is a key suppressor of hepatic gluconeogenesis. Cell Metabolism, 2021, 33: 1171-1186. DOI: 10.1016/j.cmet.2021.04.006.
Wang Y*, Wen H*, Fu JJ*, Cai L, Li PL, Zhao CL, Dong ZF, Ma JP, Wang X, Tian H, Zhang Y, Liu Y, Cai JJ, She ZG, Huang Z, Li W#, Li H#. Hepatocyte TNF receptor-associated factor 6 aggravates hepatic inflammation and fibrosis by promoting lysine 6-linked polyubiquitination of apoptosis signal-regulating kinase 1. Hepatology, 2020, 71: 93-111. DOI: 10.1002/hep.30822.
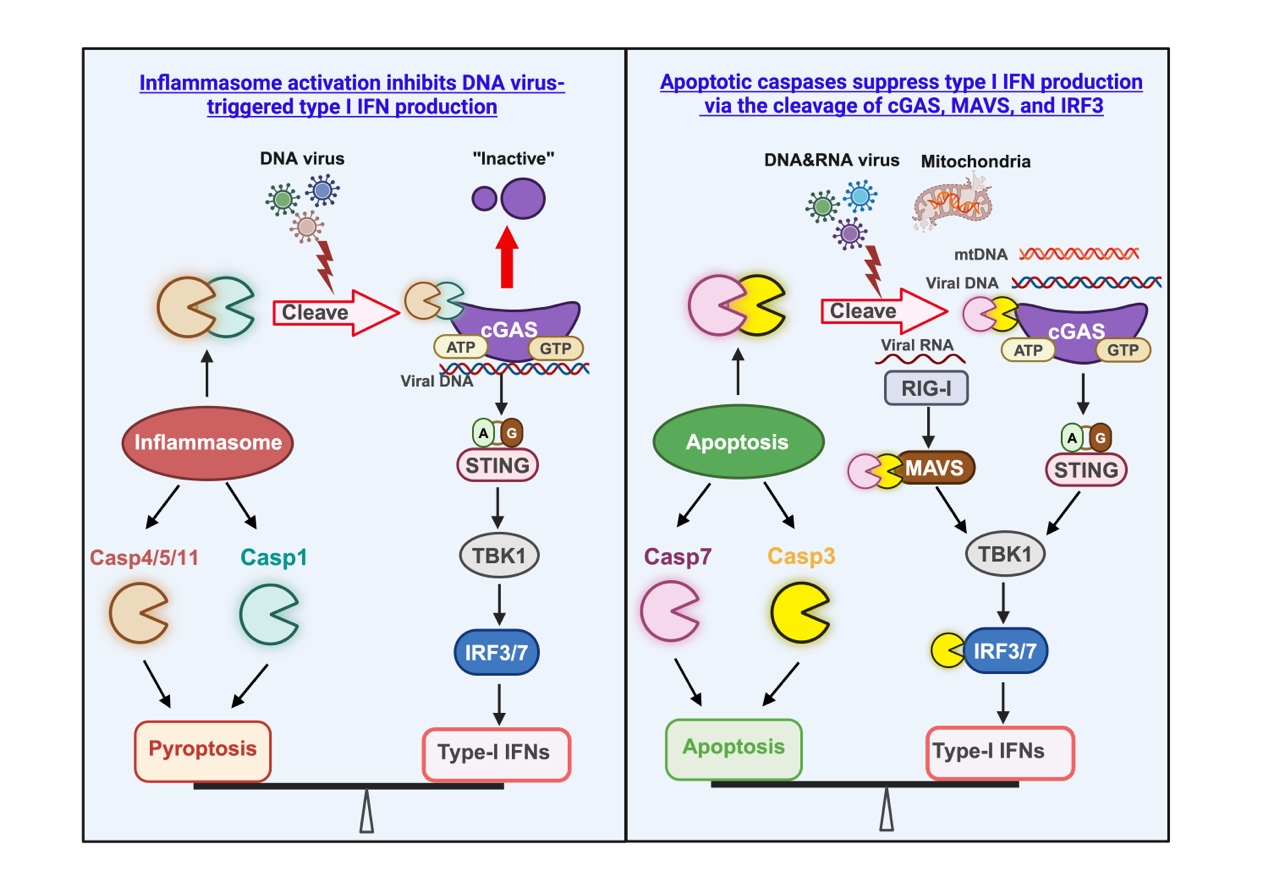
Ning X*, Wang Y*, Jing M*, Sha M, Lv M, Gao P, Zhang R, Huang X, Feng J-M, Jiang Z. Apoptotic caspases suppress type I interferon production via the cleavage of cGAS, MAVS, and IRF3. Molecular Cell, 2019, 74: 19-31. DOI: 10.1016/j.molcel.2019.02.013.
Wang Y*, Ning X*, Gao P, Wu S, Sha M, Lv M, Zhou X, Gao J, Fang R, Meng G, Su X, Jiang Z. Inflammasome activation triggers caspase-1-mediated cleavage of cGAS to regulate responses to DNA virus infection. Immunity, 2017, 46: 393-404. DOI: 10.1016/j.immuni.2017.02.011.